このページでは、シングルセルRNA-Seq(scRNA-Seq)解析の限界やデータ品質について、わかりやすく解説します。
はじめに:美しい図の「裏側」を見たことがありますか?
シングルセルRNA-Seq(scRNA-Seq)は今やオミクス解析のスタンダードです。Loupe Browserなどが描き出す色鮮やかな図は、まるで免疫染色(FISH)の画像のように、細胞の真の姿を映し出しているように見えます。
しかし、その「見映えの良さ」に騙されてはいけません。Subio Platformでデータを詳細に視覚化してみれば、そこには計算では補正しきれない「データの脆弱性」と、たまたま検出されただけの「偶然性」が横たわっていることがわかります。
1. シングルセルRNA-Seqにおけるシーケンス・デプスの問題と「細胞の個性」の虚像
これは2019年当時、シングルセルRNA-Seqが普及し始めた頃に私たちが警鐘を鳴らした内容です。
10X Genomicsなどのプロトコルでは、1細胞あたりのリード数はわずか数万程度です。通常のRNA-Seqと比較すれば、その圧倒的な少なさは一目瞭然です。
リード数が少ないということは、ダイナミックレンジ(測定できる幅)が極端に狭いことを意味します。Subio Platformでサンプルごとのread countのヒストグラムを並べてみれば、細胞ごとに「どれだけread countが得られているか」というシーケンスの深さ(デプス)に大きな差があるという事実が一目瞭然です。
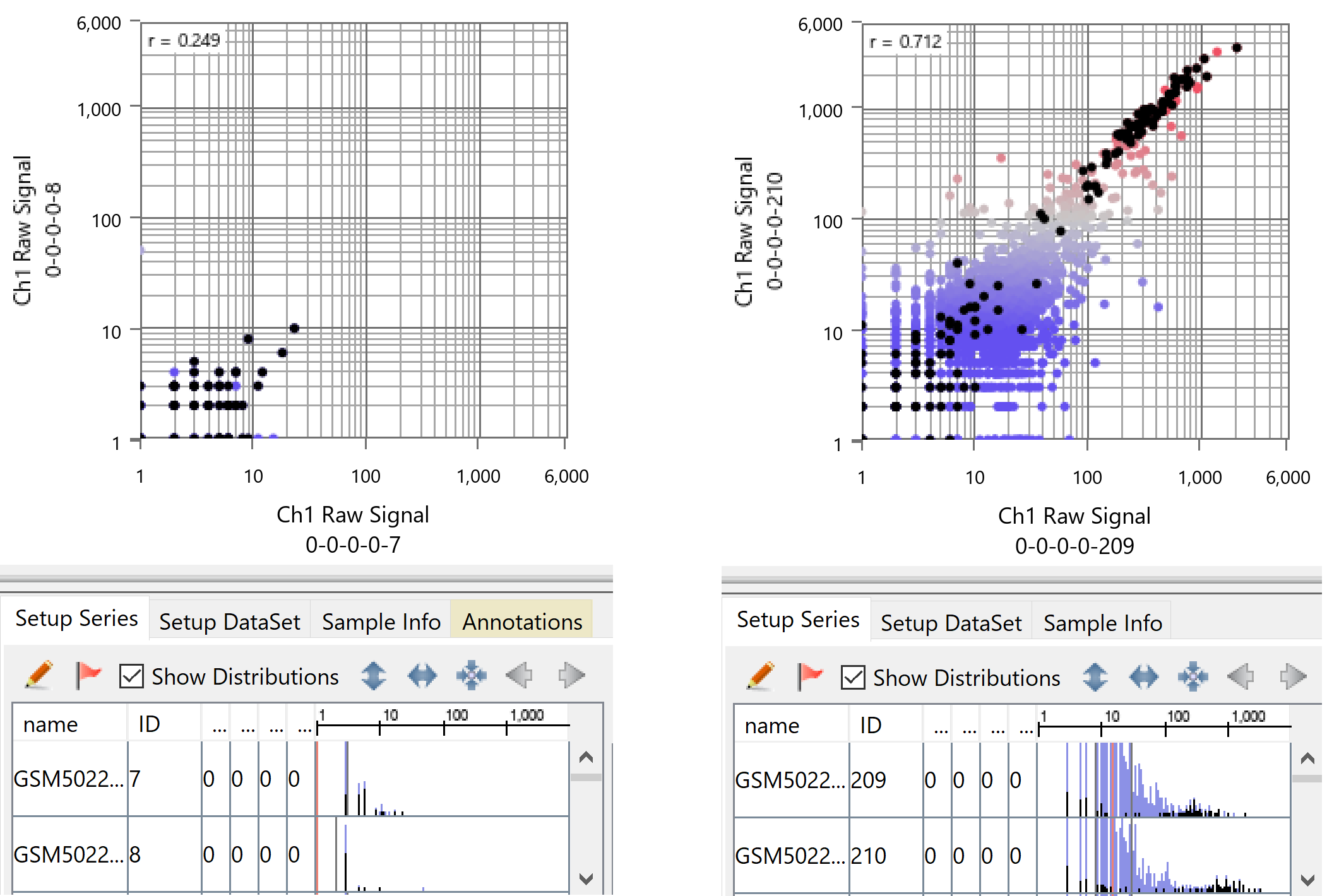
上の図は、デプスが最も浅い細胞同士と、最も厚い細胞同士を散布図で視覚化したものです(GSE164898より作成)。黒い点はribosomal protein(リボソームタンパク質)遺伝子で、本来は全細胞で超高発現しているはずのものです。この図から下記のことが明らかです。
- デプスが浅い細胞: ribosomal protein遺伝子ですら、その一部がギリギリ検出される程度しか情報がありません。
- デプスが厚い細胞: せいぜい、そのribosomal proteinと同等に超高発現している遺伝子がいくつか測定される程度です。
ここから言えることは、この技術そのものが、単なる「デプスのムラ」を「細胞の個性」へとすり替えてしまう構造的なリスクを孕んでいるということです。
そしてもう一つ、忘れてはならない大原則があります。それは「検出されなかった = 発現していない」ではないということです。単に「偶然、検出されなかった」だけかもしれないのです。
ツールが描き出すあの「美しい図」が、実はこのような非常に不安定なデータの集積によって作られている。その危うさを、私たちは知る必要があります。
2. AIに「解決策」だけを聞いてはいけない(2026年現在の視点から)
さて、ここからは2026年現在の視点でお話しします。2019年当時と決定的に違うのは、誰もがAIに解析の相談ができるようになったことです。
今、AIに「シングルセルRNA-Seqの限界は?」と尋ねれば、ある程度の答えが返ってくるでしょう。しかし、ここで一つ試してみてほしいことがあります。次に、AIへ「シングルセルRNA-Seqのバッチエフェクトを補正するには?」と聞いてみてください。AIは即座に、MNNやHarmonyといった洗練された解決手法を提示してくれるはずです。
もし、先に「品質の限界」を知らなければ、あなたはその答えをそのまま受け入れてしまうでしょう。しかし、データの根本的な「脆弱性」を知った上で見ると、ある疑問が湧くはずです。
「そもそもシグナルが欠落しているデータ同士を、計算だけで本当に『補正』できるのだろうか?」
この疑問さえ浮き上がってくれば、AIに対して「それぞれの手法の特徴や限界」をより深く、具体的に問い質すことができるはずです。解決策(How)だけを聞くのではなく、前提となる問題の構造(What)を突き合わせる。その矛盾に気づき、「本当だろうか?」という健全な疑いを持つこと。その「違和感」こそが、AI時代に生き残る(Surviveする)解析者に必須の態度、『批判的思考(クリティカル・シンキング)』です。
高度な正規化が映し出す蜃気楼
また、2019年から2026年の間に、scRNA-Seqの補正手法に関する進展もありました。デプスのムラを補正するために一般的に使われる CPM (Counts Per Million) ですが、リード数が極端に少ない細胞では、偶然の1リードの検出が大きく影響し、発現値のばらつきが増幅されることがあります。この「低入力データにおけるノイズの増幅」は、シングルセル特有の問題ではありません。ケーススタディ403で示しているように、これはbulk RNA-Seqの低発現遺伝子解析においても直面する、データ解析における普遍的な落とし穴なのです。
この問題を補正するために現在では推奨されるようになったTMM や Median-of-ratios (ただし、bulk RNA-Seq向けに設計されている)といった手法も、実際のところscRNA-Seqデータの解析においては危うい賭けです。なぜなら、洗練されたアルゴリズムが算出する「補正済みデータ」が、単純なCPMより真実に近いかどうかは、本質的に判断が難しいからです。これらの手法は「全遺伝子のうち、大半は発現が変化していない」という数学的な仮説(Assumption)に基づいた「辻褄合わせ」に過ぎません。しかし、思い出してください。scRNA-Seqで安定して検出できるのは、ごく限られた超高発現遺伝子だけです。その「観測可能なわずかな遺伝子群」だけしか見ないのであれば、その仮説の妥当性が揺らぎます。
実務家が取れる態度は、特定の手法を盲信することではなく、複数の正規化手法の結果を「並べて比較する」ことです。 どれが正解か分からないからこそ、複数の「補正データ」と「生のカウントデータ」を見比べ、データの歪みが最も少ない(あるいは納得のいく説明がつく)のはどれかを、自分の目で見極めるしかないのではないでしょうか。
ちなみに、scRNA-Seqの生データをSubio Platformで見たい場合は、GEOからmatrixファイルをダウンロードし、ChatGPTに「(ファイル名)をdense matrixのTSVに出力するPythonスクリプトを作成して。行に遺伝子、列に細胞を配置して」と依頼してみてください。生成されたスクリプトをJupyterで実行すれば、Subioに即インポート可能なファイルが完成します。AIのおかげでこうした『作業』が本当に簡単に行えるようになりましたね。詳細は別記事「ChatGPTでコード生成し、Jupyterで実行する」 も参考にしてください。
2026年時点でも scRNA-Seq はまだまだ発展途上の技術であり、その信頼性は決して盤石ではありません。「最新の高度な手法を使っているから大丈夫」と短絡的にならず、これからの技術進展(主に測定システムの感度と安定性、補正アルゴリズムではなく)に期待しつつも、常にクリティカル・シンキングの態度を忘れないでいましょう。
おわりに:自分の目で真実を峻別するために
だからこそ、Subio Platformで「自分の目」でデータを見る必要があるのです。
解析をブラックボックスにしたまま、AIが出した「もっともらしい結果」を眺めているだけでは、この違和感にすら辿り着けません。生のデータが持つ歪みや限界を、視覚を通してダイレクトに脳に刻み込む。そのプロセスを経て初めて、あなたは「ツールに使われる作業者」を脱し、AIを使いこなしながら自らの意志で結論を導き出す「真の解析者」へと進化できるのです。
Subioの考え方と対応方針
現時点のシングルセルRNA-Seqデータは、その特性上、解析結果の解釈に高度な判断が求められます。
そのためSubioでは、一定の品質や再現性を前提とした解析サービスやトレーニングの対象としては、慎重な取り扱いが必要と考えています。
だからこそ、データを「自分の目」で確認し、判断していく姿勢が求められます。
Subio Platformは、そのための解析環境です。
関連トピック
- RNA-Seqデータの品質はRNA量に依存する
(微量RNAでは通常のBulk RNA-Seqと同等の品質は得られない)