miRNA-seqとRNA-seqの違いは何か?という問いに対して、
最も重要な違いは「再現性(reproducibility)」です。
この違いは、データセット間での結果の一致性として最も明確に現れます。
遺伝子の発現量を測定する技術は、少なくとも2004年までには現在の水準に達していますので、ちゃんとしたスキルを持つ実験者により測定されたデータであれば、信頼できると言えます。一方で、マイクロRNAの発現量の測定は今なお難しいです。miRNAの発現データが、遺伝子発現データと同等に信頼できるものではないということは知っておいたほうが良いでしょう。ここでは、hepatocellular carcinoma (HCC) の複数のデータセットに跨って、遺伝子およびmiRNA発現データを見比べてみます。
RNA-Seqは再現性が高い:マイクロアレイなど異なる技術でも結果が一致する実例
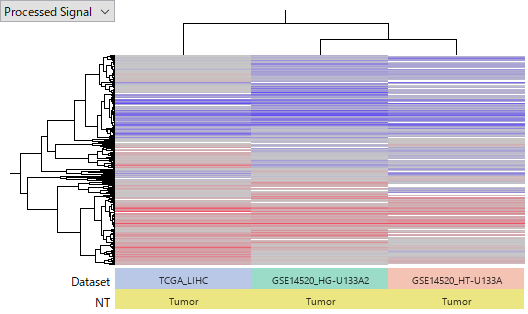
下のヒートマップは、TCGA-LIHC と GSE14520 という二つのデータセットを並べて見比べるためのものです。TCGAの遺伝子発現データは、RNA-Seqによりとられています。一方 GSE14520 はAffymetrix HG-U133A 2.0 Array と HT_HG-U133A Array という2種類のGeneChipを使って測定されたものですので、合計3つのデータセットとして扱っています。生データから処理し直して、Tumor サンプルにおける Normalサンプルに対する Log2 Ratio に変換して解析しました。赤い色はTumorで発現が亢進していることを、青色は減退していることを表します。
異なる研究者ならびに異なる手法により測定であるにもかかわらず、この3つのデータセットにおいて発現の上昇と下降がおおよそ一致しています。即ちこれらのデータの信頼性は高いといえるでしょう。
このようなデータセット間での一致性は、各データセット内での高い再現性に支えられています。
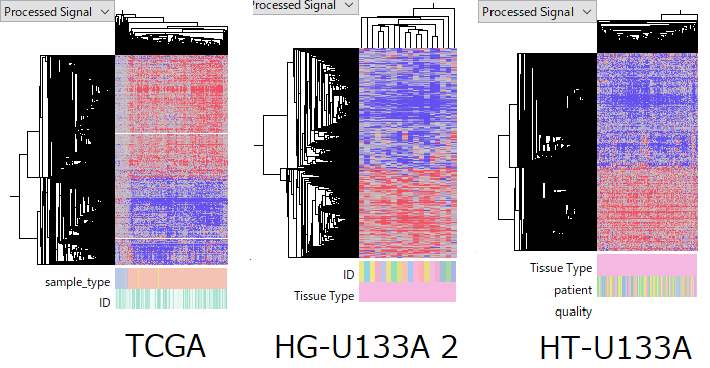
RNA-Seqはデータセット内でも再現性が高い
TCGA-LIHC RNA-Seq データセットは、50 の Normal と 370 の Tumor サンプルで構成されています。GSE14520 HG-U133A 2.0 Array データセットは、18 の Normal-Tumor ペアを含んでおり、HT-U133A データセットでは 214 ものペアを含んでいます。いくつか品質に疑問のあるサンプルが含まれるものの、全体としては質の高いデータセットと言えます。
それぞれのデータセットを見てみても、Tumor サンプルの発現プロファイルがだいたい似通っているようにみえます。これにより、これらの発現データが本来の生物学的状態を反映しているという主張に合理性をもたらします。
miRNA-seqの結果はなぜ一致しないのか:再現性が低い理由
RNA-Seqと違い、miRNA-Seqでは他者データセット間で結果がほとんど一致しないことがしばしばあります。この圧倒的なmiRNA-Seqの難しさは、miRNAの次の性質に由来します。
miRNA-seqの再現性を下げる3つの要因
配列が短く、近似度が高い
遺伝子に比べてmiRNAの塩基配列は短く(約22塩基)、ファミリー間での違いもわずか数塩基です。そのため、アレイでのクロスハイブリダイゼーションや、シーケンス解析時のマッピングの曖昧性が避けられません。
ライブラリ調製バイアス(Library Preparation Bias)
特にアダプター連結効率の差や抽出キットによる偏りが、mRNA以上に結果を左右することが分かっています。
分母(種類)が圧倒的に少ない
遺伝子に比べてmiRNAの数は非常に少なく、数千種類程度です。そのため、mRNA解析で一般的に使われる「大半の遺伝子は発現が変化しない」という前提に立つ正規化手法が通用しにくくなります。どのような計算処理をしても疑問が残りやすいため、正確な比較には 「スパイクイン(外来RNAの添加)」 による外部標準を用いた補正が必要になるケースも少なくありません。
miRNA-seqはデータセット間で再現性が低い:結果が一致しない実例
それでは、miRNA の発現データセットの実例を見てみましょう。遺伝子発現データセットのときと違い、各データセットの結果がほとんど一致していません。miRNA発現データの解釈がそう簡単にはいかないことがうかがい知れます。

miRNA-seqはデータセット内での再現性も低いことがある
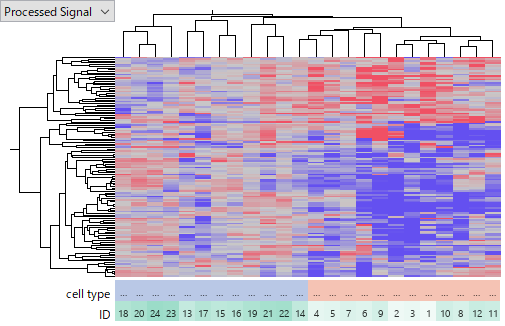
これらのデータセットで、一番大きなのはTCGA-LIHC miRNA-Seq のデータです。ヒートマップでは Tumor サンプルにおける miRNA の発現プロファイルがおおよそ一致しており、この実験がうまくいっているように見えます。

GSE110217 は、Agilent のHuman miRNA v16 microarray を使って測定されたものです。このデータセットはデータの品質に問題がありそうで、繰り返しサンプルの後半 (5 - 8) で、明らかに前半 (1 - 4) よりもシグナルが低いです。実験者のスキルが十分でなかったのではないかと考え、後半のサンプルを解析から除外しました。GSE110217は、Normal、non-HCC、HCCの3つのグループを含んでいますが、クラスタリングの結果を見るとHCCのサンプル群が右側にクラスターを形成しており、生物学的コンテキストから合理的に見えます。つまり、これも実験はうまくいっているようです。
しかし、上のデータセットを比較したヒートマップを見ると、発現上昇(あるいは下降)している miRNA がTCGAの結果をまったく一致していません。異なるプラットフォーム由来のデータセットを、miRNAの名前で名寄せして統合する際に幾分不整合があり、これにより一部でうまく比較できない可能性があるとはいえ、上の結果はあまりにも一致しなさすぎます。
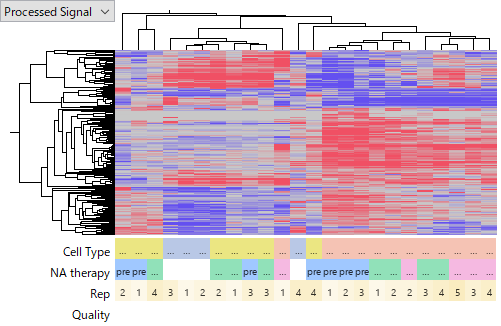
この後のヒートマップは GSE74618 (Affymetrix miRNA v2 Array)、
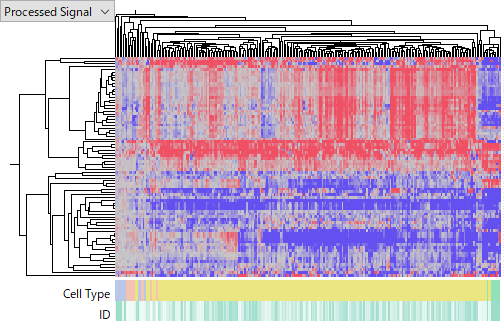
GSE115016(Affymetrix miRNA v4 Array)、
GSE10694(CapitalBio Mammalian miRNA Array)、
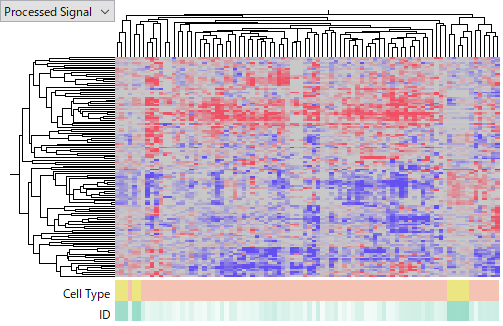
そして、GSE28854(Milteny Biotec miRXplore miRNA Microarray)の各データセットのものです。

より後のヒートマップほど、HCCサンプル間での違いが大きい、あるいはノイズの大きいデータに見えます。しかし、ここではどの測定方法が良いかを論じたいわけではありません。測定システムの良し悪しはもちろん、実験者のスキルのばらつきや、その他の見えていない要因が影響している可能性もあるからです。ここで言えるのは、miRNAの発現データは遺伝子発現データほど信頼できないということです。上の例でも、結局HCCで発現が上昇している(あるいは下降している)miRNAはどれか、という問いに答えるのがいかに難しいかわかるでしょう。
以上より、miRNAの発現量の網羅的測定は、簡単には解決できない難題を抱えている発展途上の技術といえるでしょう。miRNAのデータセットを使う時、または論文で報じられた発現上昇している(あるいは下降)しているmiRNAのリストを使う際には、十分な注意が必要です。
もし miRNA の実験を計画しているのでしたら、遺伝子発現の実験以上に高いスキルが必要だということを忘れてはいけません。
まとめ:miRNA-seq vs RNA-seq の違い
| 項目 | RNA-seq (mRNA) | miRNA-seq |
|---|---|---|
| 再現性 | 高い | 低い |
| データの一致性 | 研究間で一致 | 不一致が多い |
| 測定の安定性 | 安定 | バイアスが大きい |
| 解析の前提 | 成立する | 崩れやすい |
データをダウンロードして、Subio Platformで詳しく見てみよう
お手元の Subio Platform にデータをインポートして詳しく見てみたい方は、SOA ファイル をダウンロードしてください。SOAは、SSA ファイル を束ねたようなもので、簡単にSubio Platformにデータを展開できます。
操作:
Platform メニューからImport Archive... を開いて、ダウンロードしたSOAファイルを選択してください。インポートが完了すると自動的にSubio Platformが閉じますので、ソフトウェアを再起動してください。
【2026年追記】AIに「〇〇で発現が上昇しているmiRNAを教えて」と聞いてはいけない
このように、miRNAの発現解析は未だ多くの課題を抱えています。
近年ではAIによる解析も普及していますが、元データの品質にこれほどのバラつきがある以上、AIの出す「答え」を鵜呑みにするのは危険です。たとえば、AIに「HCC(肝細胞がん)で発現が上昇しているmiRNAを教えて」と聞くと、AIは過去の論文から抽出したリストを自信満々に提示します。 しかし、この記事が示しているのは「そもそも論文ごとに結果がバラバラで、信頼性にばらつきのあるデータが含まれている」という技術的な現実です。
また、AI(機械学習やディープラーニング)は、ノイズの多いデータでも「それらしい特徴量」を見つけ出してしまいます。たとえ生物学的には存在しないパターンであっても、それを見つけ出すように設計されているのがこれらのモデルなのです。それが生物学的に妥当かどうかを判断できるのは、AIではなく解析者自身です。
言うまでもないことですが、AIだけでなく、miRmineやmiRNAMapのような「各組織での発現量をまとめたデータベース」も、同様に注意が必要です。これらは一見便利ですが、異なる実験系のデータを無理やり統合していることが多く、そこで示される「組織差」が、実は単なる「実験手順の差」であるリスクを排除できません。
Subioは、オミクスデータに関しては、AIに直接聞くよりも、まず自分の目で直接データを確かめることをお勧めします。
Subio Platformなら、異なるデータセットを横断して比較し、このような再現性の違いを視覚的に検証することができます。